2型糖尿病(T2DM)具有复杂的“多重奏”病理生理机制,早期联合治疗是重要策略。基础胰岛素与胰高糖素样肽-1受体激动剂(GLP-1RA)同为注射剂型,两者降糖机制互补,“合二为一”为T2DM联合治疗提供了简便新方案。德谷胰岛素利拉鲁肽注射液(诺和益®)作为全球首个基础胰岛素GLP-1RA注射液,已于2021年10月26日在中国获批。这种全新的联合治疗药物有何特点?又能带来怎样与众不同的获益?本文将带您全面了解。
合二为益的创新机制
诺和益®是全球首个基础胰岛素GLP-1RA注射液,包含长效基础胰岛素类似物德谷胰岛素(100 U/ml)和GLP-1RA利拉鲁肽(3.6 mg/ml)。注射装置为3 ml预填充笔,一次注射1至50剂量单位,1剂量单位包含1单位德谷胰岛素和0.036 mg利拉鲁肽[1]。诺和益®适用于血糖控制不佳的成人 T2DM患者,在饮食和运动基础上联合其他口服降糖药物,改善血糖控制。
诺和益®两种主要成分独特的分子特性使其既可作为复方制剂,又可保持各自的药代动力学和药理特性[2],机制互补,直击T2DM“多重奏”病理生理机制[3,4]。
诺和益®作用机制视频
三大治疗优势兼顾降糖疗效和安全性
· 高达标:HbA1c<7%的患者比例可达89.9%
DUAL系列研究是诺和益®全球3期临床研究项目,分别在既往使用口服降糖药、(OAD)、GLP-1RA和基础胰岛素治疗的成人T2DM患者中观察诺和益®治疗的有效性和安全性。在所有9项研究中诺和益®组患者平均HbA1c均降至7%以下(6.0%~6.9%)(图1)[5-13]。
其中,DUAL VI研究证实,对于既往使用OAD治疗的T2DM患者,起始应用诺和益®治疗32周,HbA1c<7%的达标率高达89.9%[10]。而调查显示,我国T2DM患者单用OAD治疗的达标率仅34.6%[14],基础胰岛素治疗达标率40.6%[15]。这提示,目前我国T2DM人群血糖达标率仍不理想,诺和益®的高达标率令人期待。
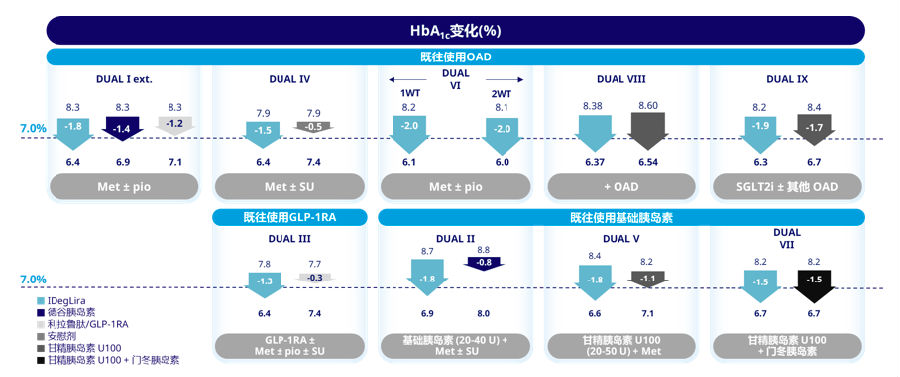
IDegLira:诺和益®;Met:二甲双胍;pio:全程健康教育;SU:磺脲类;OAD:口服降糖药;SGLT2i:钠-葡萄糖协同转运蛋白2抑制剂;GLP-1RA:胰高糖素样肽-1受体激动剂
图1. DUAL系列研究:诺和益®治疗组HbA1c均降至7%以下
· 益掌控:一天一次,有效控制全天血糖
理想的降糖药除HbA1c达标外,还应全天平稳控糖,减少血糖波动。目前国内外最新糖尿病权威指南已将葡萄糖目标范围内时间(TIR, time in range)纳入血糖控制目标(一般范围是3.9~10.0mmol/L),并建议对于大多数糖尿病患者TIR控制目标应>70%[16,17]。
诺和益®一天一次,不仅可有效控制空腹和餐后血糖,而且可实现真正24小时全面血糖控制。DUAL II和V研究一致证实,诺和益®对9-点血糖谱的改善显著优于基础胰岛素[6,9]。DUAL V和DUAL VIII研究的事后分析显示,诺和益®治疗组的患者TIR的改善优于甘精胰岛素U100组(图2)。其中,DUAL VIII研究中,治疗结束时诺和益®组平均TIR达到90%,TIR≥70%的患者比例高于甘精胰岛素U100组(图2)[18]。
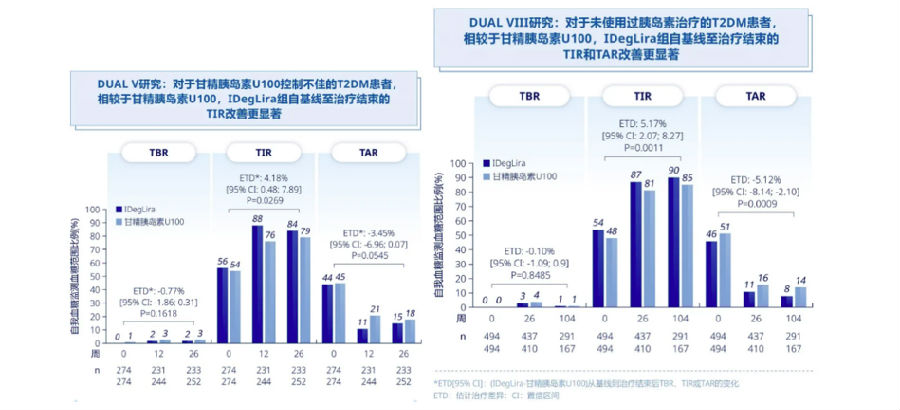
图2. DUAL V/VIII研究事后分析:诺和益®改善TIR优于甘精胰岛素U100
· 更安全:低血糖发生率低,体重获益明确
DUAL系列研究显示,诺和益®导致低血糖的风险较低(0.16~3.5事件/患者年)[6,9,13],且具有明显体重获益[6,9,11,13]。DUAL V研究(n=557)证实,治疗26周后,与甘精胰岛素U100相比,诺和益®组确证性低血糖风险降低57%(P<0.001),体重减轻(+1.8 vs. -1.4 kg,P<0.001)[9]。
适用人群:选择合适患者,临床获益更好
基于药品说明书、临床证据及治疗优势,诺和益®用于以下T2DM人群可带来治疗获益。
· 既往使用OAD治疗患者:
在既往使用OAD治疗的T2DM患者中,相比于甘精胰岛素U100,起始诺和益®治疗在胰岛素使用剂量更低的情况下降糖效果更优,达标率(HbA1c<7%)更高,低血糖风险更低,减少体重增加,且血糖控制更持久[7,13]。
· 既往使用基础胰岛素治疗患者:
在既往使用基础胰岛素治疗的T2DM患者中,相比于甘精胰岛素U100,转换为诺和益®治疗血糖达标率(HbA1c<7%)更高、胰岛素剂量更小、低血糖风险更低,体重减轻,且全天血糖控制(TIR)更好[9,18]。
· 既往使用GLP-1RA治疗患者:
在既往使用GLP-1RA治疗的T2DM患者中,与维持GLP-1RA方案不变相比,转换为诺和益®治疗可进一步显著降低HbA1c,提高血糖达标率,同时不增加方案复杂性[7]。
· 既往使用胰岛素多针治疗患者:
DUAL VII研究事后分析[19]及欧洲多中心真实世界研究[20]显示,在既往使用胰岛素多针治疗的T2DM人群中,转换为诺和益®治疗可进一步显著降低HbA1c,减轻体重,并减少胰岛素剂量,同时减少注射次数,改善糖尿病管理,改善患者依从性。
· 既往使用基础胰岛素+GLP-1RA自由联合患者:
真实世界研究显示,在既往使用胰岛素(基础/基础-餐时/预混)+GLP-1RA自由联合治疗的T2DM人群中,转换为诺和益®治疗可进一步显著降低HbA1c,并简化方案[20]。
用法用量:每日一次,剂量可调,使用简便
· 起始剂量
诺和益®起始剂量依使用人群而定,既往使用OAD患者起始剂量为10剂量单位,既往使用基础胰岛素或GLP-1RA患者起始剂量为16剂量单位(图3)[1]。
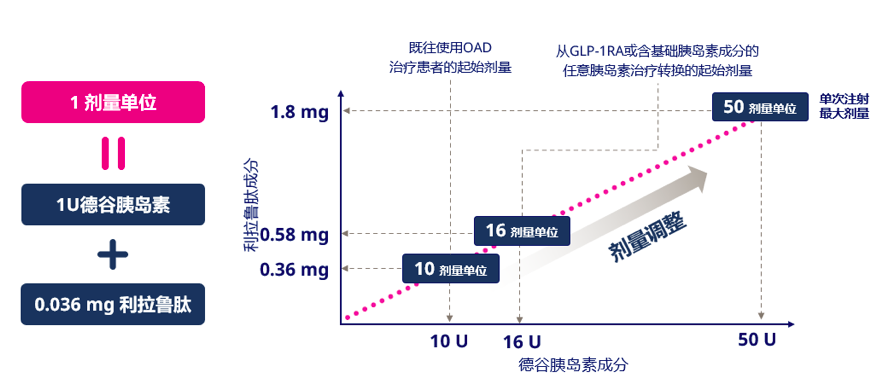
图3.诺和益®起始剂量
· 注射时间
诺和益®为无色澄清溶液,使用前不需摇匀,每日注射1次,可在一天中任意时间注射(最好在每天同一时间注射),不受进餐时间影响[1]。
遗漏用药的患者,建议他们一经发现,立即补药,并恢复常规的每日一次给药方案。两次注射之间应至少保证间隔8小时。这也适用于无法在每天的同一时间点给药的患者[1]。
· 剂量调整
诺和益®每周调整1~2次剂量,应根据患者早餐前(空腹)血糖进行调整[1]。调整方法遵循“2-0-2”原则:即患者空腹血糖高于目标值时,增加2个剂量单位;空腹血糖达标时,维持剂量不变;空腹血糖低于目标值时,减少2个剂量单位(图4)[21]。

图4. 诺和益®剂量调整
诺和益®作为全球首个、中国目前唯一的基础胰岛素GLP-1RA注射液,其成分德谷胰岛素和利拉鲁肽保留各自的药代动力学和药理特征,互补作用直击T2DM多重病理生理机制[2-4]。DUAL系列研究证实,诺和益®治疗显著降低HbA1c,HbA1c<7%的患者比例可达89.9%[10],同时低血糖风险低且体重获益明确[6,9,11,13],帮助医生和患者改善血糖管理[19]。诺和益®可在一天的任何时间(最好是每天的同一时间)注射,不受进餐时间影响 [1]。期待诺和益®早日在中国商业上市,造福更多2型糖尿病患者!
参考文献:
[1].德谷胰岛素利拉鲁肽注射液(诺和益®)产品说明书.核准日期2021年10月26日
[2].洪天配. 新视野. 2020 ;17(17) :1-3,10.
[3].Baggio L, Drucker DJ. Gastroenterology. 2007 May;132(6):2131-2157.
[4].Niswender KD. Postgrad Med. 2011 Jul;123(4):27-37.
[5].Gough SC, et al. Diabetes ObesMetab. 2015 Oct;17(10):965-973.
[6].Buse JB, et al. Diabetes Care. 2014 Nov;37(11):2926-2933. DUAL II
[7].Linjawi S, et al. Diabetes Ther. 2017 Feb;8(1):101-114. DUAL III
[8].Rodbard HW, et al. DiabetMed. 2017 Feb;34(2):189-196.
[9].Lingvay I, et al. JAMA. 2016 Mar 1;315(9):898-907. DUAL V
[10].Harris SB, et al. Diabetes ObesMetab. 2017 Jun;19(6):858-865. DUAL VI
[11].Billings LK, et al. Diabetes Care. 2018 May;41(5):1009-1016. DUAL VII
[12].ArodaVR, et al. Lancet Diabetes Endocrinol. 2019 Aug;7(8):596-605. DUAL VIII
[13].Philis-TsimikasA, et al. Philis-Tsimikaset al. Diabetes ObesMetab. 2019. 21(6):1399-1408. DUAL IX
[14].Ji LN, et al. BMC Public Health. 2013 Jun 21;13(1):602.
[15].Ji L, et al. Diabetes Obes Metab. 2017;19(8):1116-1126.
[16].中华糖尿病杂志. 2021; 13(4): 317-411.
[17].Diabetes Care. 2021; 44(Suppl 1): S1-S232.
[18].Presented at ADA 2021, 606-P.
[19].Miller E, et al. Diabetes Obes Metab. 2019 Dec;21(12):2643-2650.
[20].Price H, et al. Diabetes Obes Metab. 2018 Apr;20(4):954-962.
[21].Xultophy® Summary of Product Characteristics (SmPC), 2018.